La relación entre insuficiencia cardíaca (IC) y diabetes mellitus (DM) es bien conocida desde hace mucho tiempo. De hecho, la DM confiere un riesgo entre dos y cinco veces mayor de padecer IC, si lo comparamos con la población general. A pesar de ello, tradicionalmente, se le ha prestado menos atención que a otras complicaciones macrovasculares como la cardiopatía isquémica o la arteriopatía periférica o microvasculares como la retinopatía o la nefropatía. Ha sido en la última década y gracias a los estudios de seguridad cardiovascular de los nuevos fármacos antidiabéticos, especialmente los inhibidores del cotransportador sodio-glucosa 2 (iSGLT2), cuando la IC ha adquirido un mayor protagonismo por su frecuencia y por las implicaciones pronósticas que tiene para el paciente con DM (1).
La importancia de la insuficiencia cardíaca en la diabetes
La IC puede definirse como un síndrome complejo producido por cualquier daño estructural o funcional en el corazón que produzca una dificultad en el llenado ventricular o en la eyección de sangre.
Se pueden diferenciar varios tipos:
- IC con fracción de eyección ventricular izquierda (FEVI) reducida, si ésta se encuentra por debajo del 40%.
- IC con FEVI levemente reducida si está entre el 40-50%.
- IC con FEVI preservada cuando ésta se encuentra por encima del 50%.
Independientemente del tipo, todas ellas tienen un mal pronóstico desde el diagnóstico a pesar de las múltiples herramientas terapéuticas que se han desarrollado en los últimos años. De hecho, es una de las principales causas de hospitalización a nivel global (2).
Como se comentó previamente, la probabilidad de IC es mayor en las personas con DM, hasta dos veces mayor riesgo en el hombre y hasta cinco veces en la mujer (1). Es, por tanto, una de las complicaciones más frecuentes y mórbidas de la DM ya que además supone un mayor riesgo de hospitalización y mortalidad que en la población general. La mayoría de los datos sobre prevalencia de IC en DM de los que disponemos hoy en día se refieren a DM tipo 2 (DM2). Sin embargo, aumenta progresivamente el número de estudios que incluyen a pacientes con DM tipo 1 (DM1) puesto que la esperanza de vida para estos pacientes cada vez es mayor y, por tanto, también existen más posibilidades de seguimiento de complicaciones con tiempos de evolución muy prolongados.
EN LOS ÚLTIMOS AÑOS, Y AL IGUAL QUE HA PASADO CON MULTITUD DE ENFERMEDADES Y CONDICIONES, SE HA IDO GENERANDO UNA CRECIENTE EVIDENCIA SOBRE EL PAPEL QUE PUEDEN JUGAR LA MICROBIOTA INTESTINAL Y LAS SUSTANCIAS Y METABOLITOS QUE ESTAS BACTERIAS PRODUCEN EN LA GÉNESIS DE LA INSUFICIENCIA CARDÍACA EN PERSONAS CON DIABETES
Mecanismos por los que se afecta el corazón en la diabetes tipo 1
Al igual que en otras complicaciones cardiovasculares de la diabetes, en la aparición de IC pueden influir los factores de riesgo cardiovascular clásicos entre los que podemos destacar el control glucémico y de forma precoz desde el diagnóstico. No obstante, se ha descrito la presencia de disfunción diastólica (relajación inadecuada) en adolescentes y jóvenes con DM1, como marcador inicial de IC (3). Volviendo al control glucémico expresado como hemoglobina glicosilada (HbA1c), los datos del estudio Diabetes Control and Complications Trial (DCCT) y su estudio de seguimiento Epidemiology of Diabetes Interventions and Complications (EDIC), nos muestran que la HbA1c es un importante factor de riesgo modificable para la IC a largo plazo, de modo que cada aumento del 1% de este parámetro aumenta hasta tres veces el riesgo de IC (4). Del mismo modo, la aparición de otros factores asociados a la DM como son la albuminuria, el mal control de la tensión arterial o la enfermedad renal crónica, aumentan el riesgo de IC de forma considerable. Debemos tener en cuenta que, sobre todo la enfermedad renal crónica, aparece con más frecuencia en la DM1 debido al largo tiempo de exposición a la enfermedad pues se diagnostica de forma más precoz que la DM2. Por otra parte, la prescripción de fármacos que controlan factores de riesgo como antihipertensivos, hipolipemiantes o antiagregantes es menos frecuente en la DM1, pudiendo también contribuir a este riesgo aumentado de IC.
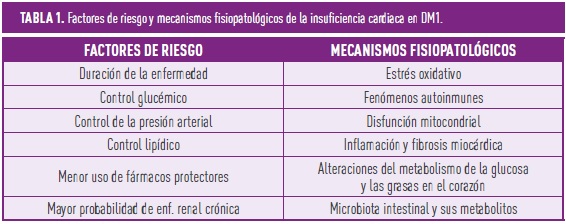
Entrando más a fondo en los mecanismos fisiopatológicos específicos de la DM1, podemos destacar algunos como el estrés oxidativo por la producción de radicales libres de oxígeno, las alteraciones locales del metabolismo de la glucosa o las grasas a nivel cardíaco, la disfunción mitocondrial observada en el tejido cardíaco de los pacientes con DM1, la infiltración del miocardio por células inflamatorias que favorecen la fibrosis o los fenómenos de autoinmunidad, también incrementados en este grupo de pacientes (2). En la tabla 1 quedan representados los principales factores de riesgo y mecanismos fisiopatológicos que favorecen el mayor riesgo de IC en el paciente con DM1.
¿Qué papel juega la microbiota intestinal?
De forma añadida a lo que hemos explicado anteriormente, en los últimos años, y al igual que ha pasado con multitud de enfermedades y condiciones, se ha ido generando una creciente evidencia sobre el papel que pueden jugar la microbiota intestinal y las sustancias y metabolitos que estas bacterias producen en la génesis de la IC en personas con DM1. Si bien es cierto que los datos son aún escasos y en ocasiones discordantes, sí parece claro que las personas con DM1 presentan un perfil microbiano diferente a la población general y a las personas con otros tipos de DM no mediadas por fenómenos autoinmunes. Se ha reportado también un incremento de la producción de citoquinas proinflamatorias y de la permeabilidad intestinal en pacientes con DM1 (5).
Existen diferentes mecanismos por los que la microbiota intestinal podría favorecer la insuficiencia cardíaca y otras enfermedades cardiovasculares, como por ejemplo la modulación de la inmunidad intestinal. Algunas bacterias como Bacteroides Fagilis promueven la producción de sustancias antiinflamatorias que podrían relacionarse con una disminución del remodelado ventricular. También algunos estudios han mostrado que bacterias como Akkermansia, Prevotella o Phascolarctobacterium se podrían asociar a cambios en la función y la estructura cardíaca. Por otra parte, parece que la insuficiencia cardíaca juega también un papel fundamental en la disbiosis por un aumento de la permeabilidad intestinal y la traslocación bacteriana, pues la reducción del gasto cardíaco podría dañar la barrera intestinal (2). Este fenómeno de permeabilidad intestinal está también incrementado en la DM1, como dijimos previamente.

A fin de no perdernos con filos, géneros y familias de bacterias, centraremos la atención en un enemigo común que aparece frecuentemente implicado en la enfermedad metabólica y cardiovascular, el N-óxido de trimetilamina o TMAO. El TMAO se forma a partir de la conversión bacteriana de trimetilamina, un producto de desecho que deriva de la descomposición de algunos nutrientes como la colina o la carnitina. Se produce fundamentalmente en el hígado, se libera a la sangre y se elimina principalmente por vía renal. Varios estudios han demostrado que niveles elevados de TMAO pueden favorecer la acumulación de colesterol en las paredes arteriales y la formación de placas de ateroma, promoviendo la enfermedad coronaria, la cardiopatía isquémica o la enfermedad cerebrovascular (6). De hecho, TMAO parece ser un factor pronóstico para la aparición de eventos cardiovasculares y de mortalidad, así como para la aparición y progresión de trombosis, inflamación crónica de bajo grado o enfermedad renal crónica. Todas ellas son factores de riesgo para la IC de etiología isquémica o no isquémica (7).
Pues bien, también se ha estudiado la utilidad de los niveles de TMAO en la predicción de complicaciones cardiovasculares y renales en pacientes con DM1. En un estudio publicado por Winther et al. midieron los niveles de TMAO en 1159 pacientes con DM1 y recogieron datos sobre la mortalidad de origen cardiovascular, los eventos cardiovasculares y la enfermedad renal durante un periodo de seguimiento medio de 15 años. Encontraron que mayores niveles de TMAO se relacionaban con la mortalidad por todas las causas y la mortalidad cardiovascular en los pacientes con DM1, independientemente de los factores de riesgo clásicos. En cuanto a la IC, los niveles elevados de TMAO fueron un factor predictor de IC (recogieron 81 eventos de hospitalización por IC). Por tanto, concluyen que el TMAO podría ser un factor de riesgo derivado de la microbiota independiente para enfermedad cardiovascular y renal en personas con DM1 (8). Se trata de un único estudio observacional, pero con una muestra de pacientes muy amplia y si bien se necesitan más estudios para dilucidar todos los mecanismos implicados, sí parece que el TMAO puede tener un papel central en la fisiopatología de la IC en DM1.

Referencias.
- Shaw JA, Cooper ME. Contemporary Management of Heart Failure in Patients with Diabetes. Diabetes Care. 2020 Dec;43(12):2895–903.
- Gómez-Perez AM, Damas-Fuentes M, Cornejo-Pareja I, Tinahones FJ. Heart Failure in Type 1 Diabetes: A Complication of Concern? A Narrative Review. JCM [Internet]. 2021 Sep 29 [cited 2023 May 11];10(19):4497. Available from: https://www.mdpi.com/2077-0383/10/19/4497
- Ifuku M, Takahashi K, Hosono Y, Iso T, Ishikawa A, Haruna H, et al. Left atrial dysfunction and stiffness in pediatric and adult patients with Type 1 diabetes mellitus assessed with speckle tracking echocardiography. Pediatr Diabetes. 2021 Mar;22(2):303–19.
- Diabetes Control and Complications Trial (DCCT)/Epidemiology of Diabetes Interventions and Complications (EDIC) Study Research Group. Intensive Diabetes Treatment and Cardiovascular Outcomes in Type 1 Diabetes: The DCCT/EDIC Study 30-Year Follow-up. Diabetes Care. 2016 May;39(5):686–93.
- Leiva-Gea I, Sánchez-Alcoholado L, Martín-Tejedor B, Castellano-Castillo D, Moreno-Indias I, Urda-Cardona A, et al. Gut Microbiota Differs in Composition and Functionality Between Children With Type 1 Diabetes and MODY2 and Healthy Control Subjects: A Case-Control Study. Diabetes Care. 2018 Nov;41(11):2385–95.
- Gątarek P, Kałużna-Czaplińska J. Trimethylamine N-oxide (TMAO) in human health. EXCLI Journal; 20:Doc301; ISSN 1611-2156 [Internet]. 2021 [cited 2023 May 11]; Available from: https://www.excli.de/index.php/excli/article/view/3239
- Tang WHW, Li DY, Hazen SL. Dietary metabolism, the gut microbiome, and heart failure. Nat Rev Cardiol [Internet]. 2019 Mar [cited 2023 May 11];16(3):137–54. Available from: http://www.nature.com/articles/s41569-018-0108-7
- Winther SA, Øllgaard JC, Tofte N, Tarnow L, Wang Z, Ahluwalia TS, et al. Utility of Plasma Concentration of Trimethylamine N-Oxide in Predicting Cardiovascular and Renal Complications in Individuals with Type 1 Diabetes. Diabetes Care [Internet]. 2019 Aug 1 [cited 2023 May 11];42(8):1512–20. Available from: https://diabetesjournals.org/care/article/42/8/1512/36150/Utility-of-Plasma-Concentration-of-Trimethylamine