El tratamiento de la diabetes tipo 1 (DM1) ha experimentado avances significativos en los últimos años gracias a los sistemas de administración automática de insulina (AID). Sin embargo, los sistemas actuales aún requieren de intervención manual para el anuncio de comidas o de ejercicio, lo que limita su capacidad para imitar la fisiología pancreática de manera óptima. El desarrollo de sistemas de asa cerrada total (fully closed-loop, FCL) busca eliminar estas limitaciones, ya que ofrece un control glucémico completamente automatizado y adaptado a las necesidades individuales sin necesidad de instrucciones previas. Este artículo analiza los avances recientes que se dieron a conocer durante el congreso Advanced Technologies & Treatment for Diabetes (ATTD) 2025, que tuvo lugar del 19-22 de marzo en Amsterdam, Países Bajos.
Avances hacia el Fully Closed-Loop
1. Enfoques bihormonales:
Los sistemas bihormonales representan un enfoque prometedor para imitar de manera más precisa la fisiología pancreática, ya que combinan insulina con otras hormonas como glucagón o pramlintida (análogo de amilina).
- Insulina + glucagón: este sistema bihormonal totalmente reactivo que no requiere de anuncios de ingestas o ejercicio, ha demostrado su eficacia para mejorar el tiempo en rango (TIR). Sin embargo, para que el dispositivo funcione correctamente, el paciente debe realizar un gran esfuerzo, ya que el glucagón debe reconstituirse y los dos sensores de que consta deben calibrarse.
- Insulina + pramlintida: este enfoque utiliza pramlintida, un análogo de la amilina, para mejorar el control postprandial. La pramlintida es secretada por las células beta y ayuda a mitigar las excursiones glucémicas después de las comidas. Estudios de fase 2 han mostrado resultados prometedores con formulaciones combinadas de insulina glargina y pramlintida o en combinación con AID (en 2 dispositivos por separado), lo que demuestra su viabilidad y eficacia.
2. Enfoques multi-hormonales:
El control postprandial sigue siendo un punto débil, incluso con sistemas avanzados. Los anuncios de comida y los errores en la cronología (timing) del bolo afectan el TIR, requiriendo estrategias automatizadas que no dependan del usuario. Los enfoques multi-hormonales (asocian a insulina liraglutida y/o pramlintida, semaglutida, tirzepatida) ofrecen mejores resultados en glucemias postprandiales y menor necesidad de insulina prandial en comida y cena, siendo útiles como refuerzo postprandial, ya que también asocian pérdida de peso y ofrecen un perfil postprandial más plano.
3. Sistemas basados solo en insulina:
Aunque más simples que los bihormonales, los sistemas basados exclusivamente en insulina enfrentan retos relacionados con el retraso en la absorción y, por tanto, de la acción de la insulina subcutánea, así como el retraso fisiológico que comporta la detección de glucosa intersticial respecto a la capilar (5-15 min).
- Insulinas ultrarrápidas: las nuevas formulaciones buscan acelerar la acción de la insulina para responder de forma más eficaz a la variabilidad glucémica. A pesar de que mejoran la glucemia postprandial y el TIR, su impacto no parece que sea clínicamente significativo (más marcado en el desayuno y la cena que en el almuerzo).
- Administración intraperitoneal (IP): esta vía permite una acción más rápida y una mayor captación hepática de insulina, reduciendo así el riesgo de hipoglucemia. Además, los sensores IP detectan cambios glucémicos mucho antes que los subcutáneos, y los estudios in silico confirman la viabilidad de combinar sensores + infusión IP con algoritmos de control. Actualmente, se está desarrollando un páncreas artificial totalmente implantable con sensor + bomba IP + algoritmo en smartphone.
- Algoritmos avanzados: tecnologías como el Bolus Priming System (BPS) detectan automáticamente comidas no anunciadas en función de la velocidad de ascenso de glucosa y ajustan la dosis de insulina en tiempo real, ejecutándose cada 5 minutos y mejorando significativamente el TIR en entornos controlados.
4. Sistemas DIY (Do-It-Yourself):
Los sistemas DIY, como Loop, AndroidAPS y Trio, representan una comunidad de innovación abierta donde los usuarios adaptan y mejoran los sistemas AID existentes, permitiendo ajustes dinámicos y personalizados. Estos sistemas utilizan algoritmos como Super Micro Bolus (SMB), Oref o UAM (UnAnnounced Meals) que mejoran el control posprandial sin necesidad de bolos manuales, demostrando una alta satisfacción en usuarios DIY y un apoyo creciente desde las sociedades médicas.
EL FUTURO DEL MANEJO DE LA DIABETES ESTÁ CADA VEZ MÁS CERCA GRACIAS A LOS AVANCES TECNOLÓGICOS Y AL PODER TRANSFORMADOR DE LA INTELIGENCIA ARTIFICIAL, ABRIENDO NUEVAS VÍAS PARA UN CONTROL GLUCÉMICO MÁS PRECISO Y PERSONALIZADO
La comunidad DIY ha liderado la implementación de estrategias avanzadas y ha demostrado que es posible lograr un control glucémico altamente personalizado. Sin embargo, su complejidad técnica limita su adopción masiva, por lo que se debe trabajar para hacerlas fácilmente enchufable y usable (plug and play). Se está haciendo un esfuerzo creciente para integrar estas innovaciones en sistemas comerciales y hacerlas más accesibles.
En este sentido, la Food and Drug Administration ha comenzado a aprobar algoritmos desarrollados por la comunidad open-source, como es el caso de Loop, abriendo nuevas vías para la innovación, la regulación de estos sistemas y fomentando la co-creación y colaboración entre pacientes y desarrolladores.
LOS SISTEMAS BIHORMONALES REPRESENTAN UN PASO CRUCIAL HACIA UN CONTROL AUTÓNOMO Y FISIOLÓGICO, PERMITIENDO A LAS PERSONAS CON DM1 DESPREOCUPARSE DE LAS INGESTAS Y EL EJERCICIO
Inteligencia artificial: La clave del futuro
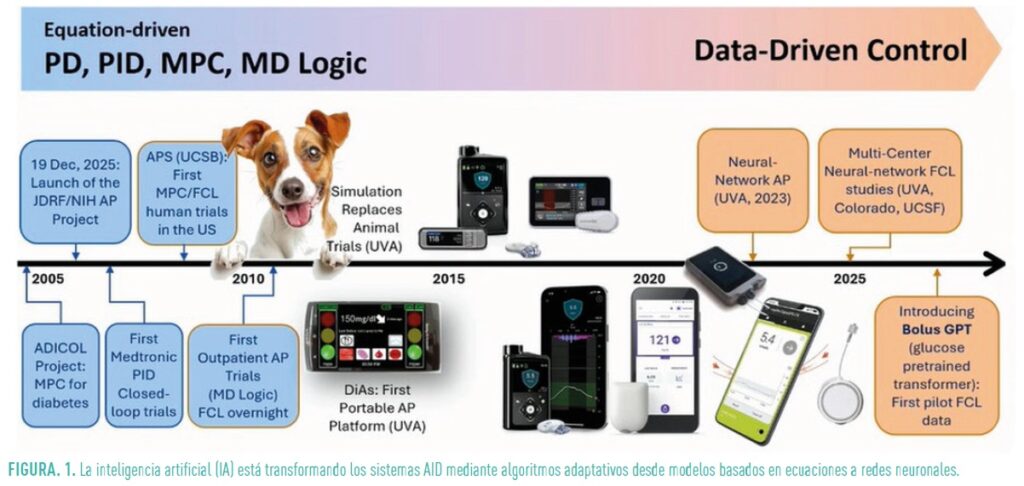
La inteligencia artificial (IA) está transformando los sistemas AID mediante algoritmos adaptativos que aprenden continuamente del comportamiento individual del usuario (Fig.1).
- NAP@home: este sistema basado en redes neuronales ha demostrado ser seguro y eficaz en condiciones reales, mejorando el TIR sin aumentar hipoglucemias. Los resultados de NAP@home muestran la transición de algoritmos basados en ecuaciones a modelos de datos, apostando por algoritmos personalizados y adaptativos.
- Machine Learning: algoritmos como Bolus GPT predicen necesidades de insulina con alta precisión, marcando una transición hacia un control verdaderamente automatizado. El aprendizaje basado en simulaciones permite anticipar las necesidades de insulina, ofreciendo resultados prometedores, aunque con un número reducido de participantes.
Retos pendientes
A pesar de los avances significativos, alcanzar un Fully Closed-Loop plantea desafíos importantes:
- Control postprandial: las comidas mixtas siguen siendo un reto debido a su impacto variable en la glucosa (efecto pizza). Los algoritmos actuales no reconocen la composición nutricional de las comidas, necesitando estrategias automatizadas que no dependan del usuario.
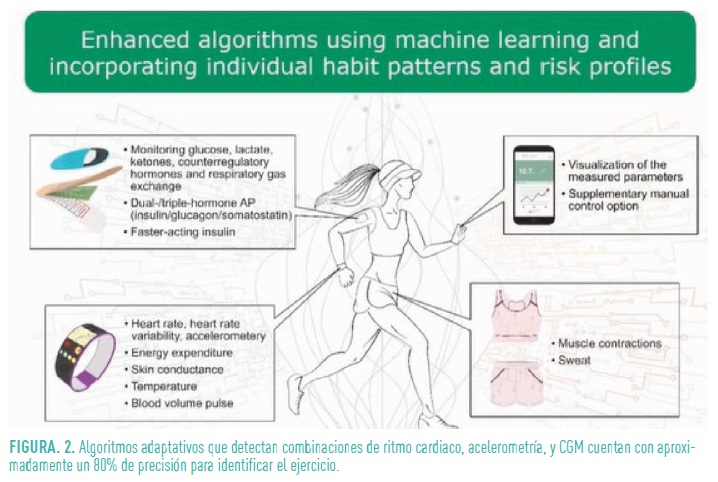
- Ejercicio físico no planeado: los cambios en la glucosa asociados al ejercicio no planeado requieren de la implementación algoritmos adaptativos que puedan anticiparse a estas variaciones por medio de la detección de una combinación de ritmo cardiaco, acelerometría, y CGM, con un 80% de precisión (Fig. 2).
- Accesibilidad y sostenibilidad: es crucial garantizar que estas tecnologías sean accesibles para todas las personas con DM1, independientemente de su ubicación geográfica o situación económica, promoviendo una estrategia global que incluya innovación, acceso y sostenibilidad.
Conclusiones
El desarrollo de sistemas Fully Closed-Loop supone una revolución tecnológica en el tratamiento de la diabetes tipo 1. Aunque aún quedan retos por superar, los avances en inteligencia artificial, algoritmos avanzados y nuevas vías de administración acercan cada vez más este objetivo. Estos dispositivos tienen el potencial de mejorar significativamente el control metabólico y de liberar a las personas con diabetes del estrés asociado a la gestión diaria de su enfermedad, lo que promovería una mejor calidad de vida y un mayor bienestar.
Referencias
- Renard E. Automated insulin delivery systems: from early research to routine care of type 1 diabetes. Acta Diabetol. 2023 Feb;60(2):151-161. doi: 10.1007/s00592-022-01929-5. Epub 2022 Aug 22. PMID: 35994106.
- Bekiari E, Kitsios K, Thabit H, Tauschmann M, Athanasiadou E, Karagiannis T, Haidich AB, Hovorka R, Tsapas A. Artificial pancreas treatment for outpatients with type 1 diabetes: systematic review and meta-analysis. BMJ. 2018 Apr 18;361:k1310. doi: 10.1136/bmj.k1310. PMID: 29669716; PMCID: PMC5902803.
- Qiao YC, Ling W, Pan YH, Chen YL, Zhou D, Huang YM, Zhang XX, Zhao HL. Efficacy and safety of pramlintide injection adjunct to insulin therapy in patients with type 1 diabetes mellitus: a systematic review and meta-analysis. Oncotarget. 2017 Mar 8;8(39):66504-66515. doi: 10.18632/oncotarget.16008. PMID: 29029531; PMCID: PMC5630431.
- Dassau E, Renard E, Place J, Farret A, Pelletier MJ, Lee J, Huyett LM, Chakrabarty A, Doyle FJ 3rd, Zisser HC. Intraperitoneal insulin delivery provides superior glycaemic regulation to subcutaneous insulin delivery in model predictive control-based fully-automated artificial pancreas in patients with type 1 diabetes: a pilot study. Diabetes Obes Metab. 2017 Dec;19(12):1698-1705. doi: 10.1111/dom.12999. Epub 2017 Jul 6. PMID: 28474383; PMCID: PMC5742859.
- Moscoso-Vasquez M, Colmegna P, Barnett C, Fuller M, Koravi CLK, Brown SA, DeBoer MD, Breton MD. Evaluation of an Automated Priming Bolus for Improving Prandial Glucose Control in Full Closed Loop Delivery. Diabetes Technol Ther. 2025 Feb;27(2):93-100. doi: 10.1089/dia.2024.0315. Epub 2024 Nov 6. PMID: 39501832..
- Wilmot EG, Danne T. DIY artificial pancreas systems: the clinician perspective. Lancet Diabetes Endocrinol. 2020 Mar;8(3):183-185. doi: 10.1016/S2213-8587(19)30416-4. PMID: 32085824..
- Braune K, Hussain S, Lal R. The First Regulatory Clearance of an Open-Source Automated Insulin Delivery Algorithm. J Diabetes Sci Technol. 2023 Sep;17(5):1139-1141. doi: 10.1177/19322968231164166. Epub 2023 Apr 13. PMID: 37051947; PMCID: PMC10563523.
- Kovatchev B, Castillo A, Pryor E, Kollar LL, Barnett CL, DeBoer MD, Brown SA. Neural-Net Artificial Pancreas: A Randomized Crossover Trial of a First-in-Class Automated Insulin Delivery Algorithm. Diabetes Technol Ther. 2024 Jun;26(6):375-382. doi: 10.1089/dia.2023.0469. PMID: 38277161; PMCID: PMC11305265.
- Bihormonal fully closed-loop system for the treatment of type 1 diabetes: a real-world multicentre, prospective, single-arm trial in the Netherlands. van Bon, A C et al. The Lancet Digital Health, Volume 6, Issue 4, e272 – e280







