1. Introducción
El uso de las nuevas tecnologías aplicadas a la diabetes tipo 1 (DM 1) ha transformado definitivamente, en los últimos años, el manejo de la misma, llegando a formar parte indispensable de su tratamiento integral, independientemente de la modalidad de tratamiento (múltiples dosis de insulina -MDI- o sistemas de infusión subcutánea continua de insulina -ISCI). Tanto los nuevos sistemas de liberación de insulina como los dispositivos de monitorización de la glucosa (MCG) están contribuyendo, claramente, a optimizar el control glucémico de los pacientes con DM1, mejorando en muchos casos tanto su calidad de vida como la de sus cuidadores, particularmente en el ámbito de la edad pediátrica. Así mismo, el desarrollo y perfeccionamiento de estas tecnologías ha permitido el acceso a los sistemas de “asa cerrada” o páncreas artificial.
A lo largo de este artículo intentaremos dar una visión general, pero a la vez actualizada y crítica, del panorama actual de las nuevas tecnologías aplicadas a la DM1, incluyendo expectativas de futuro.
2. Sistemas de administración de insulina
- La disponibilidad de plumas de insulina con capacidad para administrar 0,5 Unidades (U) de insulina, tanto recargables, como desechables ya ha supuesto una mejora significativa en el control de la diabetes en los niños pequeños. El siguiente paso ha sido convertir una pluma de insulina tradicional en una pluma inteligente; conectándola un dispositivo móvil que permite, entre otras cosas, monitorizar las dosis de insulina administradas, controlar la temperatura de la insulina, sincronizarse con sistemas de monitorización de glucosa, o actuar como calculador de bolos. Actualmente, existen diferentes plumas inteligentes como son la pluma Pendiq® 2.0, muy útil en pediatría ya que permite administrar dosis de 0,1 en 0,1 U a partir de 0,5 U, el sistema Insulclock®, que consiste en un capuchón que se coloca sobre plumas desechables, o la recientemente comercializada pluma InPen®, sincronizada con el monitor continuo de glucosa Guardian Connect®.
- Otros dispositivos que han demostrado mejoría en cuanto al control clínico y a la adherencia al tratamiento son los puertos para la administración de insulina subcutánea. Permiten la infusión de insulina a través de una cánula de plástico que está localizada en tejido subcutáneo y que se cambia cada 3 días. En España disponemos del Iport ® e Insuflón®.
- Finalmente, un breve recordatorio de los sistemas ISCI, conocidos como “bombas de insulina”, en los que se dispone de una infusión continua programada de insulina así como de la posibilidad de administrar bolos para las comidas o para las correcciones de hiperglucemia. Además, utilidades como calculadores de bolos, diferentes formas de administración de estos, basales temporales, etc. otorgan ayuda para mejorar la gestión de la diabetes. La mayoría de estos sistemas llevan un catéter: Minimed® 640/670/780G, Roche Insight®, Tandem t-slim®. Existen también bombas sin catéter, conocidas como “bombas parche”, como son la bomba Solo® de Roche o la bomba Omnipod (no disponible en España)
El tratamiento con ISCI ha demostrado una mejora significativa en el control clínico y la calidad de vida de los de pacientes con diabetes de cualquier edad. La posibilidad de administrar dosis muy pequeñas de insulina ha permitido optimizar el tratamiento, especialmente en niños muy pequeños, incluidos lactantes y neonatos. Sus principales limitaciones son la propia incomodidad de llevar el sistema adherido a la piel y siempre “encima”, lo que produce rechazo fundamentalmente en adolescentes, así como el posible desarrollo de alergias o infecciones cutáneas.
El futuro de ISCI es, por un lado, la mejoría de la infusión de insulina con sistemas más pequeños, sin catéteres, más precisos y más cómodos. Y por otro lado su futuro está ligado al desarrollo de los sistemas de asa cerrada (ver apartado 4)
3. Sistemas de monitorización de glucosa (MCG): ¿qué miden? ¿Son fiables?
El conocimiento de los niveles de glucosa sigue siendo esencial para el manejo adecuado de la DM1. En este sentido, la revolución tecnológica de las últimas décadas ha permitido el paso progresivo del control glucémico mediante glucemia capilar (GC) a la monitorización de glucosa, bien de forma continua (MCG), o bien a demanda o intermitente, también denominado sistema “flash” (iMG), en el que vemos los datos sólo cuando pasamos el receptor o el móvil. Ambos sistemas han demostrado su precisión y utilidad en la optimización del control metabólico y, en algunos casos, han sido aceptados como válidos sin requerir comprobación de la GC, salvo en circunstancias especiales. También existen sistemas de monitorización ciegos o retrospectivos, en los que los datos pueden ser analizados con posterioridad por el equipo diabetológico, conocidos como sistemas profesionales de MCG, aunque nos centraremos en los MCG a tiempo real.
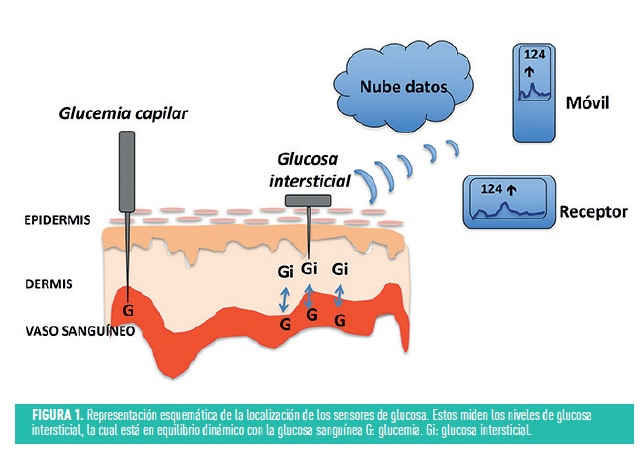
La MCG nos informa indirectamente de las cifras de glucosa sanguínea de manera continua, así como de sus fluctuaciones y tendencias en un momento dado. Las flechas de tendencia no solo predicen los niveles de glucosa en los próximos 30 min, sino que también informan, y este aspecto es de gran utilidad, de su velocidad de cambio. La MCG mide la glucosa en el líquido intersticial cada 1 a 5 minutos, mediante unos filamentos denominados sensores que se introducen debajo de la piel, en el tejido subcutáneo; generalmente brazo, glúteos o abdomen (figura 1). Es muy importante destacar que la glucosa intersticial es distinta de la glucosa en sangre capilar, por lo que los valores pueden no coincidir, sobre todo en momentos de cambio rápido de la glucemia, teniendo un retraso variable con la medición real, aproximadamente de unos 10-12 min, dependiendo de la glucemia y su velocidad de cambio en ese momento. Este hecho se interpreta con frecuencia, erróneamente, como falta de fiabilidad del sensor, siendo crucial instruir adecuadamente a los pacientes y familiares.
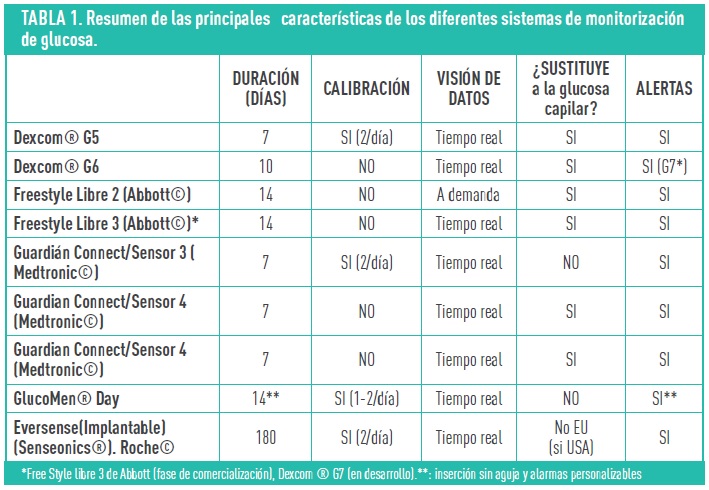
Las prestaciones generales de diferentes dispositivos quedan resumidos en la tabla 1. Disponen además de un transmisor que envía la señal al receptor (monitor, bomba de insulina, teléfono móvil o la nube de datos), donde podemos ver el valor y perfil de la glucosa, así como las flechas de tendencia (figura 1). En la actualidad, y debido al grado de precisión alcanzado, muchos de los sistemas de MCG no precisan la comprobación de la glucemia capilar, salvo en determinadas circunstancias (es decir, no hay que calibrarlos) y han demostrado beneficios clínicos significativos tanto en la modalidad de tratamiento con MDI como en los tratados con ISCI.
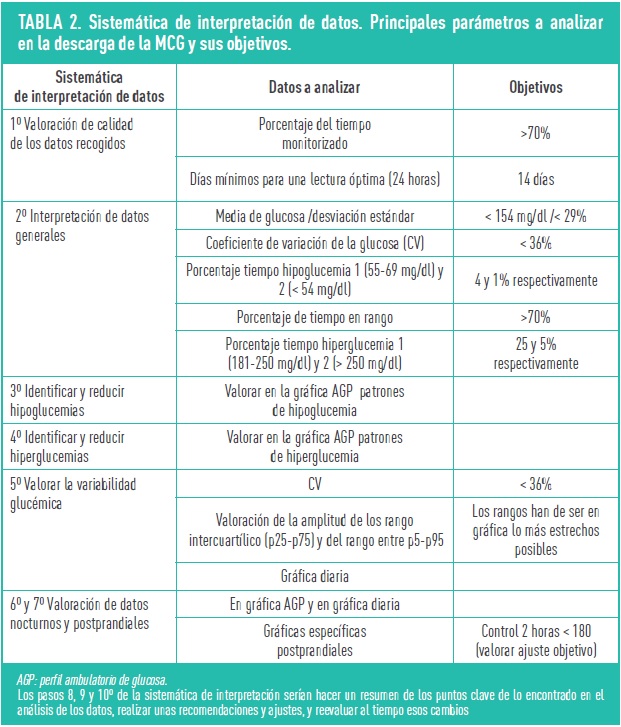
La valoración de los datos obtenidos mediante los diferentes sistemas de MCG han cambiado la manera de interpretar el control de la glucosa y, en muchas ocasiones, el protocolo de actuación. La estandarización de los sistemas de descarga de datos (tabla 2), ha permitido la descarga de mediciones globales y evaluación de objetivos, así como establecer estrategias sistematizadas para evaluarlos y generar recomendaciones de actuación, en base a las evidencias clínicas hasta el momento actual.
El futuro de los sistemas de MCG está centrado en aumentar su precisión y exactitud (especialmente en hipoglucemia), disponer de alarmas individualizadas, eliminar la necesidad de calibración, mejorar el sistema de visualización e interpretación de datos, disminuir su invasividad, incrementar su duración y estar adaptados para situaciones que requieren estudios radiológicos.
En la actualidad, se encuentran en fase de desarrollo y/o reciente comercialización el FreeStyle 3 (Abbot ©), más pequeño y delgado, con diseño más sostenible frente al medio ambiente, y el Dexcom® G7 desechable y también de menor tamaño en relación con modelos previos.
Otros progresos que se están llevando a cabo en estos sistemas consisten en el desarrollo de aplicaciones que detecten cuándo una persona está comiendo, evitando así el problema del olvido de bolos, especialmente importante en la población adolescente. En la actualidad, existen estudios en marcha con algunas aplicaciones (KLUE) programadas en un Apple Watch®, capaces de detectar bolos perdidos y enviar alertas de texto al usuario, según los movimientos de la mano dominante en los que se reconocen acciones como llevarse comida a la boca.
4. Sistemas integrados o de liberación automática de insulina
El desarrollo tecnológico de los sistemas de asa cerrada, que unen a la MCG con la administración automática de insulina vía ISCI, ha transformado también el tratamiento de la DM1.
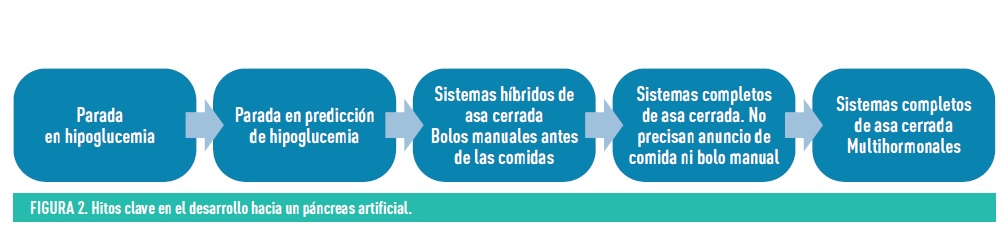
Los primeros sistemas que ofrecían automatismo fueron los sistemas integrados que suspendían la infusión de la insulina basal en hipoglucemia o ante la predicción de una hipoglucemia (figura 2).
Un paso adelante ha sido el desarrollo de sistemas con administración automática de insulina vía ISCI. Constan de tres componentes: MCG, ISCI y un algoritmo matemático de control o controlador. Este algoritmo matemático determina la cantidad de insulina a infundir en función de los valores de glucosa intersticial a tiempo real, siendo, de esta forma, la administración de insulina automática y más parecida a la liberación fisiológica. Casi todos los sistemas de asa cerrada actuales precisan la administración, por parte del usuario, de los bolos previos a las comidas, por lo que se los conoce como sistemas híbridos de asa cerrada al no ser completamente automáticos.
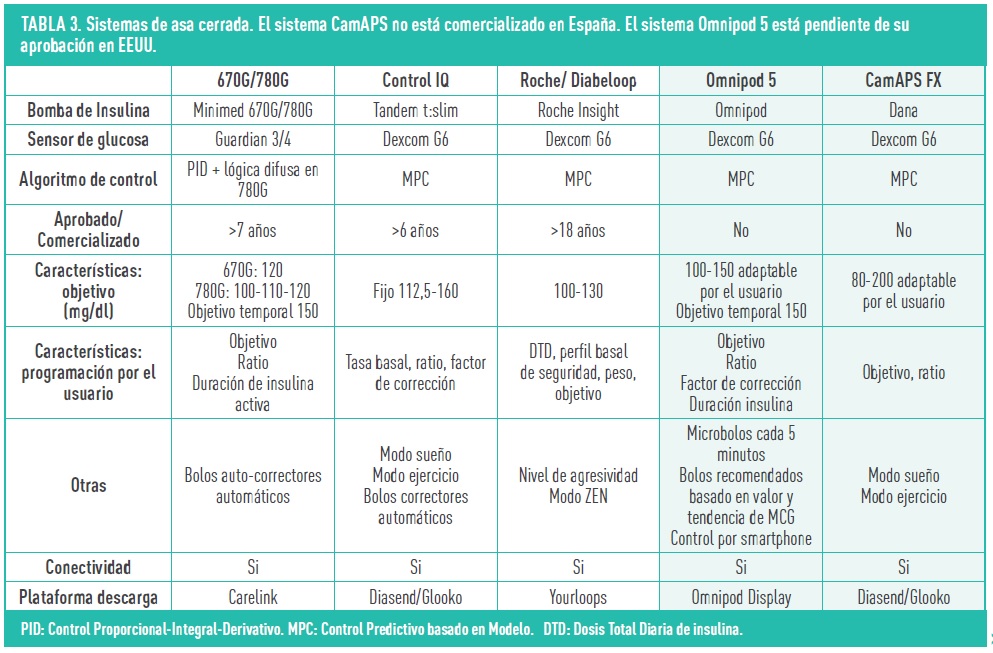
Actualmente hay dos sistemas aprobados en España para uso pediátrico: Minimed® 670G/780G y Tandem Control IQ®. El sistema Diabeloop de Roche© está disponible para su uso en mayores de 18 años. Los sistemas CamAPS y Omnipod 5 no están comercializados en España, este último pendiente de su aprobación por la FDA en EEUU. El algoritmo puede estar localizado en el propio infusor de insulina o en un dispositivo móvil externo.
A pesar de su uso reciente, ya han sido publicados diferentes trabajos en los que se ha demostrado su beneficio clínico. Se ha observado una mejoría del control clínico con un aumento del tiempo en rango sin aumento del tiempo en hipoglucemia, una mejoría significativa del control glucémico nocturno, así como una mejoría de la calidad del sueño y de vida de los niños y de sus cuidadores. Recientemente, ha sido publicado un estudio en dos niños de 7 y 18 meses de edad en el que el sistema CamAPS® ha demostrado ser eficaz y seguro. Para poder optimizar este tipo de terapia en niños tan pequeños se ha necesitado recurrir a la insulina diluida.
Las hiperglucemias posprandiales siguen siendo un problema en los sistemas híbridos, al depender del paciente la administración del bolo prepandial y el recuento de los hidratos de carbono. El manejo de la actividad física constituye otro reto, al cambiar de forma significativa la sensibilidad a la insulina y aumentar el riesgo de hipoglucemias, precisando, aún con este tipo de terapia, tener un plan de ejercicio o “anunciarlo” al sistema. Posibles mejoras a estos dos aspectos serían la utilización de insulinas de acción aún más rápida, o la posibilidad de integrar monitores de frecuencia cardíaca o acelerómetros para poder detectar, lo antes posible, el inicio de la actividad física. Esto sería muy útil en niños ya que la actividad física no suele ser programada.
Los sistemas de asa cerrada bihormonales o páncreas duales permiten añadir glucagón al sistema de infusión de insulina. El uso del glucagón agrega una protección adicional ante las hipoglucemias y permite ser más agresivo a la hora de tratar las hiperglucemias. Sin embargo, añade complejidad al sistema ya que precisa de dos sistemas de infusión independientes. Otra posibilidad de páncreas dual es añadir pramlintida, que reduce la hiperglucemia postprandial enlenteciendo el vaciado gástrico. Incluso se plantean a futuro, páncreas trihormonales con insulina, glucagón y pramlintida.
5. Plataformas de descarga de datos.
La posibilidad de descargar tanto los datos del sensor como de las “bombas” o, de que estos datos “suban a la nube” desde diferentes dispositivos electrónicos: bomba, móvil o receptor, y que el profesional sanitario, al igual que el paciente y su familia, pueda acceder a ellos abre muchas posibilidades de mejora del control de la diabetes. Cada casa comercial dispone de una plataforma para la descarga de datos (tabla 3). En estas plataformas se incluyen diferentes parámetros estadísticos: perfil ambulatorio de glucosa (AGP), gráficas de perfil diario de glucosa, perfil semanal, patrones de hipo e hiperglucemia, etc. Para poder analizar todos los datos se recomienda seguir una sistemática de interpretación de estos (tabla 2). En el año 2017, las diferentes sociedades científicas unificaron las recomendaciones a dar y los objetivos a conseguir. Es importante que el paciente y sus familiares realicen la interpretación de estos datos con cierta periodicidad para así poder optimizar el tratamiento.
6. Telemedicina.
La telemedicina (posibilidad de realizar medicina a distancia mediante recursos tecnológicos) ha aumentado su visibilidad y uso durante la pandemia COVID19. Permite que el paciente acuda al centro sanitario sólo si es necesario, lo que añade nuevas posibilidades al modelo tradicional. La utilidad de la telemedicina en la diabetes ya ha sido demostrada. Sin embargo, la transformación hacia una telemedicina de calidad debe venir acompañada de seguridad jurídica, capacitación digital de los profesionales y de los pacientes, reconocimiento del tipo de actividad asistencial por parte del sistema sanitario y disponibilidad por parte de los pacientes de tecnologías que permitan el control remoto siendo la MCG fundamental para poder realizar una telemedicina de calidad.
7.- Peculiaridades del uso de nuevas tecnología en el niño pequeño (menores de 5 años)
Los niños pequeños con DM1, sobre todo los menores de 5 años, tienen unas características peculiares que los convierten en un grupo especialmente complejo y vulnerable. Con mayor frecuencia debutan con cetoacidosis diabética, así como niveles inferiores y deterioro más rápido de reserva pancreática. Además, presentan mayor variabilidad glucémica, mayor sensibilidad y duración de la insulina, mayor dificultad para adaptar la terapia al ejercicio y dificultades para la dosificación de sus requerimientos de insulina, tanto en MDI como en ISCI o sistemas híbridos. A pesar de haberse objetivado una mejoría en el control clínico con los sistemas híbridos en este grupo etario, siguen existiendo algunas limitaciones para su manejo:
- Bolos prandiales tardíos, lo que implica una hiperglucemia inicial que activa al sistema haciendo que haya una mayor administración de insulina con una hipoglucemia posterior.
- Se necesita una dosis diaria mínima para optimizar el sistema.
- Se necesita confiar en el sistema para obtener el máximo beneficio.
Por tanto, aspectos específicos como determinados parámetros técnicos, tanto de los sistemas de MCG como de los sistemas de infusión de insulina (dosificación mínima, objetivos temporales, alarmas, obstrucciones del catéter, etc), facilidad de uso y tamaño del dispositivo son de vital importancia para el control de su diabetes, mejorando así el grado de satisfacción y estrés familiar.
La menor precisión de los sistemas de MCG en rango de hipoglucemia y la frecuencia considerable de problemas dermatológicos asociados al uso de la MCG constituyen áreas de estudio y mejora para este grupo de pacientes.
8.- ¿Existen robots humanoides al servicio del paciente con diabetes?
Dado que los niños y adolescentes aceptan muy bien las nuevas tecnologías, los robots humanoides podrían ofrecer una nueva opción para ayudar a los pacientes pediátricos con DM1. De hecho, ya existen algunos artículos que propugnan que el uso de robots humanoides asistidos podría ayudar en manejo de la DM1, actuando especialmente como “gestores” de la enfermedad, educadores y comunicadores, ofertando también apoyo emocional. En general, aunque los estudios no son homogéneos metodológicamente, parece que podrían tener un impacto positivo en el área afectiva, de relación, cognitiva y de comportamiento. Aunque atractivo y prometedor, se necesitan todavía nuevas evidencias en este campo.
9.- ¿Qué deben saber los médicos generales y pediatras?
Las nuevas tecnologías no solo han revolucionado nuestra sociedad, sino también el manejo de la DM1, incrementando su complejidad y haciendo necesaria la continua actualización.
En este sentido, es de vital importancia que los médicos y pediatras, incluso la enfermería escolar, dispongan de unos conocimientos generales de los distintos dispositivos y pautas de monitorización, así como del tratamiento de la DM1.
Estos conocimientos deberían incluir cuestiones como: ¿qué es una bomba de insulina y cómo funciona?, ¿qué son los sistemas de MCG?, ¿cómo actuar en situaciones agudas: hipo e hiperglucemia? La existencia de protocolos sencillos diseñados por el equipo diabetológico para su uso en estos foros y situaciones, así como una comunicación periódica y fluida entre Atención Primaria, centro escolar y equipo diabetológico constituye la clave para ofrecer una buena atención al paciente con DM1.
Conclusiones
Las nuevas tecnologías aplicadas a la DM1, en constante cambio y progreso, constituyen un área prometedora que intenta dar respuesta a las distintas necesidades de los pacientes, con el objetivo de contribuir a la optimización del control glucémico, a la par que disminuir la carga de la enfermedad, tanto a los pacientes como a los familiares, mejorando así su futuro y calidad de vida. Los nuevos dispositivos para pacientes con MDI así como los sistemas de ISCI y los sistemas de MCG han hecho posible el desarrollo de los sistemas híbridos y el poder contar con sistemas de “asa cerrada híbridos“. La mejora de programas de descarga y el desarrollo de la telemedicina están contribuyendo a facilitar la atención tanto de los pacientes con DM1 como de sus familiares. El desarrollo de “apps” novedosas, capaces de reconocer acciones, permitiendo enviar alertas al paciente, así como robots humanoides podrán, eventualmente, contribuir a mejorar el control y la calidad de vida de los pacientes con DM1, sin olvidar la piedra angular de la educación diabetológica.
Bibliografía
- Battelino T, Danne T, Richard M. Bergenstal RM, Amiel SA, Beck R, et al. Clinical Targets for Continuous Glucose Monitoring Data Interpretation: Recommendations. From the International Consensus on Time in Range. Diabetes Care 2019; 42(8): 1593–1603.
- Galindo RJ and Aleppo G. Continuous Glucose Monitoring: the achievement of 100 years of innovation in diabetes technology. Diabetes Res Clin Pract 2020; 170: 108502. doi:10.1016/j.diabres.2020.108502.
- Leelarathna L, Choudary P, Wilmot EG, Lumb A, Street T, Kar P et al. Hybrid Closed loop therapy. Where are we in 2021? Diabet Obes Metab 2021;23:655-60.
- Dos Santos TJ, Costa-Rodriguez T, Puñales M, Arrais RF and Kopacek C. Newest Diabetes-Related Technologies for Pediatric type 1 Diabetes and Its Impact on Routine Care: a narrative synthesis of the literature. Current Pediatrics Reports 2021. doi: 10.1007/s40124-021-00248-7.
- Nevo-Shenker M, Moller P, Nimri R and Shalitin S. Type 1 diabetes mellitus management in young children: implementation of current technologies. Pediatric Research 2020; 624–629.
- Lau Y, Hui-Chee DG, Chow XP, Wong SH, Cheng L J, Lau ST. Humanoid robot-assisted interventions among children with diabetes: A systematic scoping review. International J Nursing Studies 2020; https://doi.org/10.1016/j.ijnurstu.2020.103749
- Fuchs J and Hovorka R (2021) Benefits and challenges of current closed-loop technologies in children and young people with type 1 diabetes. Diabetes. Front. Pediatr. 9:679484
- Tseretopoulou X, Viswanath V, Hartnell S, Ware J, Thankamony A et al. Safe and effective use of a hybrid closed-loop system from diagnosis in children under 18 months with type 1 diabetes. Pediatr Diabetes. 2021;1-8.
- Petrovski G, Al Khalaf F, Campbell J, Umer F, Almajaly D, Hamdan M. One‑year experience of hybrid closed-loop system in children and adolescents with type 1 diabetes previously treated with multiple daily injections: drivers to successful outcomes. Acta Diabetologica (2021) 58:207–213
- Messer L, Berget C, Pyle L, Vigers T, Cobry E, Driscoll K, Forlenza G. Real-world use of a new hybrid closed loop improves glycemic control in youth with typ1 diabetes. Diabet Technol Ther 2021 Dec;23(12):837-843