La monitorización intersticial de glucosa (MIG) constituye una herramienta imprescindible de evaluación del control glucémico, ofreciendo gran cantidad de datos. Para la interpretación de los datos, tenemos que evaluar las 7 métricas refrendadas por el consenso internacional de tiempo en rango (TIR) y el perfil de glucosa ambulatorio (AGP). Parámetros como TIR, tiempo por encima o por debajo del rango (TAR y TBR), coeficiente de variación (CV), indicador de gestión de glucosa (GMI) entre otros, han pasado de ser parte exclusiva de protocolos de investigación a formar parte del día a día de cualquier consulta de diabetes. Sin embargo, aunque está claro que la MIG ofrece una alternativa a la HbA1c al permitir una valoración integral de los niveles de glucemia intersticial de forma continuada, su interpretación no está exenta de dificultades.
Los 7 parámetros glucométricos definidos en el consenso de MCG, presentan una alta interdependencia entre sí, y el intento de mejora de uno de ellos puede suponer el empeoramiento del resto, dificultando la interpretación y optimización de los tratamientos para conseguir un buen control glucémico. Por otro lado, la evaluación simultánea de los diferentes parámetros del informe de la AGP y del registro diario de la MIG requiere experiencia, tiempo y sin duda una curva de aprendizaje por parte del equipo sanitario y supone una carga de trabajo para el personal que atiende personas con diabetes. El TIR recientemente se ha consolidado como variable esencial de control metabólico y se ha relacionado con complicaciones crónicas micro y macrovasculares, equiparando un TIR > 70% a un buen control metabólico y a una HbA1c 7% en pacientes con DM1 Y DM2. Si bien, el uso aislado del TIR no presenta suficiente sensibilidad ni en la valoración de la hipoglucemia ni para los valores extremos de glucosa y por tanto de la variabilidad glucémica (VG). Por tanto, no se puede simplificar el análisis de la MIG utilizando exclusivamente el TIR. Por ello, parece lógico buscar nuevos parámetros que permitan sintetizar los datos existentes y orientar a los profesionales en el manejo de la DM1, especialmente aquellos con menos experiencia.
EL TIR RECIENTEMENTE SE HA CONSOLIDADO COMO VARIABLE ESENCIAL DE CONTROL METABÓLICO Y SE HA RELACIONADO CON COMPLICACIONES CRÓNICAS MICRO Y MACROVASCULARES, EQUIPARANDO UN TIR > 70% A UN BUEN CONTROL METABÓLICO Y A UNA HBA1C 7% EN PACIENTES CON DM1 Y DM2
INDICE DE RIESGO GLUCÉMICO
El Índice de Riesgo Glucémico (GRI) se describe por primera vez en el año 2022 y pretende resumir en un único parámetro la calidad global del control glucémico de un determinado paciente (1). Su cálculo surge del análisis de las diferentes puntuaciones otorgadas por 330 expertos internacionales en DM1 a los datos de MCG de 225 pacientes con diabetes tratados con insulina (1). Las puntuaciones de los expertos dependían de dos componentes: componente de hipoglucemia (Chipo) y componente de hiperglucemia (CHiper). La suma de estos dos componentes ponderados por unos coeficientes permite el cálculo del GRI, teniendo en cuenta que el GRI pondera de forma más importante la hipoglucemia (TBR) y los valores extremos (1).
GRI= 3,0 × [+TBR<54 + (0,8 × TBR 54-70)] + 1,6 × [TAR>250 + (0,5 ×TAR 180-250)]
El GRI evalúa el control glucémico global de un paciente otorgando una puntuación de 0 a 100 puntos, siendo 0 el mejor control y 100 el peor control posible. Además, puede categorizarse y representarse gráficamente mediante percentiles (Pc) en cinco zonas que van desde el mejor (Pc 0-20) al peor (Pc 80-100) control glucémico, facilitando la visualización de sus resultados, así como la identificación de los puntos clave para mejorar y controlar los efectos sobre la calidad glucémica. Como se infiere de su fórmula, el GRI permite la valoración simultánea y ponderada de dos componentes esenciales del control metabólico como son el TBR y el TAR (y por tanto indirectamente en relación con el TIR), dando mayor peso al TBR y en concreto a los valores glucémicos extremos (1). Los primeros autores que incorporaron el GRI en la práctica clínica habitual demuestran una mejoría del GRI tras implementar el tratamiento con sistemas de liberación automatizada de insulina (AHCL). Nuestro grupo en una muestra de 137 pacientes (65 pediátricos) demuestra un mejor control en población pediátrica expresado a través de GRI, pero con un mayor componente de hipoglucemia (2). Queda aún por determinar si el GRI tendrá relación con las complicaciones de la diabetes. Se describe un mayor riesgo de retinopatía diabética a mayor GRI, aumentando un 20% el riesgo de esta por cada aumento de percentil del GRI (3). Así también se demuestra una asociación fuerte entre GRI y distintos indicadores de nefropatía diabética (3). En cuanto a la relación del GRI con otros parámetros glucométricos, en nuestro grupo demostramos que el GRI se correlaciona significativamente con todas las métricas analizadas, especialmente con el TIR (fuerte correlación negativa r=-0.917), y además la VG afecta la correlación del GRI con otros parámetros (2). La HbA1c y el GRI muestran una correlación fuertemente positiva, que se ve modificada por la variabilidad glucémica (CV) (2).

El GRI muestra ventajas al ser de cálculo sencillo y fácil de automatizar, y engloba el control metabólico en un solo parámetro en una escala de 0 a 100. Tiene una representación gráfica sencilla e intuitiva, es un parámetro sencillo a la hora de priorizar o controlar la evolución de un mismo o de diferentes pacientes y ofrece una valoración con trasfondo clínico y no exclusivamente matemático, pudiendo evaluar los cambios a lo largo de tiempo. Pero, presenta escasa evidencia en la práctica clínica diaria, con ausencia de un valor de normalidad o deseable y además no es calculado automáticamente en las plataformas de MCG, no existiendo datos validados en población pediátrica y gestación, lo cual frena su uso generalizado. El GRI podría ser especialmente interesante en aquellos equipos sanitarios con menos experiencia en MCG o a la hora de priorizar mediante un parámetro único y de manera sencilla aquellos pacientes que podrían beneficiarse de determinadas intervenciones al permitir comparar rápidamente tanto pacientes independientes como la evolución de un mismo paciente.
TIEMPO EN RANGO ESTRECHO
El tiempo en rango estrecho o time in tight range (TITR) se define como el tiempo que la glucosa permanece entre 70 y 140 mg/dl. La necesidad del TITR surge a raíz de los datos de MIG en personas sanas. El 85% de las personas sanas estudiadas tenían menos del 5% de valores de > 140 mg/dl, pasando la mayor parte del tiempo entre 70-140 mg/dl y alcanzando raramente niveles entre 140 y 180 mg/dl y si lo hacen es sólo por un periodo corto de tiempo tras las comidas. La hipoglucemia y la hiperglucemia son peligrosas para el desarrollo y funcionamiento cerebral, existiendo cada vez más estudios que describen los efectos de la disglicemia en la barrera hematoencefálica y el riesgo de demencia, y el impacto de la hipo e hiperglucemia en la cognición y en el desarrollo cerebral en niños pequeños con DM1. Parece por tanto importante mantener la normoglucemia para preservar la función cerebral en todas las edades. Pero sin duda el TITR ha surgido ante la aparición de nuevos tratamientos que han permitido no sólo mejorar el control metabólico, sino conseguir valores de glucosa lo más próximos a la normalidad posible. Desde el consenso internacional de TIR en 2019 existe discusión relativa a la necesidad de ajustar los rangos de glucosa. Los rangos de glucosa se determinaron mediante esfuerzos de consenso para alinearse con las definiciones utilizadas antes de la introducción de la MCG, pero no se basaron en resultados clínicos, en ese momento el objetivo terapéutico de una Hba1c inferior a 7% fue equiparada a un TIR 70-180 mg/dl del 70%. Algunos autores han propuesto que el TITR puede reflejar mejor las métricas de MCG de normoglucemia, y los valores normales de glucemia, representando un tiempo más estrecho y fisiológico.

1.-Utilidad del TITR. El TITR refleja mejor los valores de glucosa normal, y ya se empieza a hablar de nuevas denominaciones como TING (time in normoglycemia) y TINR (time in normoglycemic range). Diferentes estudios en vida real (4,5) demuestran que la implementación de sistemas AHCL en pacientes con DM1 mejora el control metabólico tanto en población pediátrica como adulta, pero a expensas de mejorar el TITR es decir el tiempo en normoglucemia (70-140mg/dl), no modificándose el tiempo entre 140-180 mg/dl. En el caso de pacientes con DM2 el TITR puede identificar precozmente el diagnóstico de estadios precoces, ya que en normoglucemia el TIR y el TITR son muy similares con HbA1c 5 %, pero con HbA1c entre 5,5 Y 6,5 % la diferencia la marca el TITR al ser claramente inferior al TIR (6).
2.- Objetivos TITR. Parece que un TITR > 50% puede ser una meta de tratamiento razonable y segura en DM1. Ya Peterson en 2019 estableció que un TITR 50% corresponde a una HbA1c 6,5 %, siendo corroborado posteriormente por Castañeda que establece que un TITR 45% sería equiparable a una HbA1c <7% (5). Existe debate en el objetivo de TITR a conseguir, e incluso si establecer diferentes objetivos de TITR en función de la franja horaria (objetivo nocturno superior). Es más fácil conseguir TITR superiores a menor evolución de la enfermedad (reciente diagnóstico, periodo de remisión o luna de miel), así como en DM2 al tener menor variabilidad glucémica y menor TBR. El tipo de tratamiento también influye en el TITR, consiguiendo mejor TITR aquellos pacientes en tratamiento con AHCL. Battelino et al (7) en un consenso internacional de MCG y métricas para ensayos clínicos sugieren un objetivo de TITR > 70% para personas con DM1 en tratamiento con AHCL y DM2 en tratamiento farmacológico reductor de glucosa, porcentaje muy similar a las recomendaciones de TIR. Este objetivo tan estricto no se cumple en ninguno de los estudios realizados en vida real, algunos de los cuales tiene un porcentaje de TITR >70% tan bajo como un 1,9%. Existe por tanto debate en cuanto a los objetivos a marcar de TITR. La ISPAD establece un objetivo de TITR ≥ 50% y este objetivo también ha sido descrito como alcanzable en niños preescolares con acceso a un equipo sanitario con experiencia y acceso a tecnología. Sin embargo, este objetivo puede ser difícilmente alcanzable en pacientes sin acceso a tecnologías avanzadas, y algunos autores han descrito que en individuos con DM1 que no utilizan dispositivos capaces de prevenir la hipoglucemia se recomienda un objetivo de TITR del 40% (8).
EL TITR REFLEJA MEJOR LOS VALORES DE GLUCOSA NORMAL, Y YA SE EMPIEZA A HABLAR DE NUEVAS DENOMINACIONES COMO TING (TIME IN NORMOGLYCEMIA) Y TINR (TIME IN NORMOGLYCEMIC RANGE)
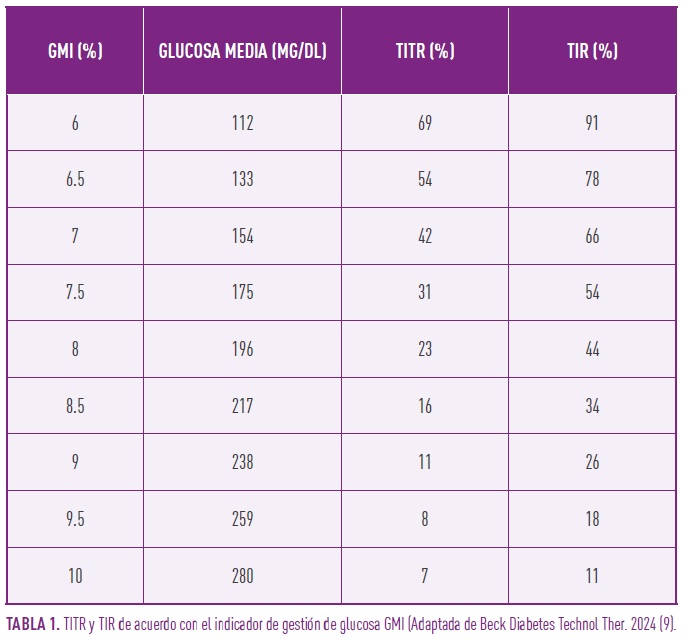
3.-Correlación con otros parámetros. Se ha descrito que existe una correlación no lineal fuertemente positiva entre TIR Y TITR. (4). La relación TIR/TITR está influida por la VG: a mayor VG expresada por CV mayor es el TITR que corresponde a un determinado TIR (4,9). También existe una correlación positiva entre TITR y HbA1c. El TITR en promedio es 20-25% más inferior que el TIR cuando el GMI está entre 6-8% en distintas cohortes y con diferentes tratamientos. La diferencia entre TITR y TIR se estrecha con valores más altos de Hba1c (9). (Tabla 1).
4.- En quién utilizar TITR. Aunque TIR y TITR son complementarios, el TITR será preferible al TIR en aquellos pacientes en los que el objetivo es la normoglucemia (HbA1c < a 5,7 o 6%), ya que en esos niveles el TIR es insensible a cambios en glucemia media y CV. En esos casos el TITR ayuda a los pacientes a ser conscientes y visualizar excursiones adicionales por encima del rango objetivo comparado con TIR. El control glucémico estrecho es el objetivo en embarazadas y niños (larga expectativa de vida, memoria metabólica) y en estadios precoces de diabetes (estadio 1 y 2). En estos pacientes debería utilizarse el TITR.
5.- Como afecta a nuestros pacientes la utilización de TITR. Entre los posibles inconvenientes de utilización del TITR en los pacientes encontramos los siguientes:
- Más riesgo de hipoglucemia.
- Mayor nivel de ansiedad. ¿Estaremos introduciendo un nuevo nivel de ansiedad, relacionado con la necesidad de vigilancia constante para conseguir un objetivo más estrecho? En una encuesta realizada a 19 padres y 11 adolescentes con DM1, reconocen que la implementación del TITR les supuso una mayor carga y un mayor nivel de estrés, junto a un mayor esfuerzo por estar dentro de objetivos (en rango estrecho).
- Utilizar como objetivo el TITR puede resultar en un mayor número de alarmas, pudiendo mitigarse mediante una configuración robusta de las mismas.
6.-Relación con complicaciones. El TIR ha demostrado estar fuertemente asociado con complicaciones tanto macro como microvasculares. Debido a la correlación no lineal entre TIR y TITR se supone que un incremento en el TITR se asociará a una menor tasa de complicaciones a largo plazo. En los últimos años están surgiendo estudios que relacionan el TITR con el riesgo de complicaciones. Así, se describe un aumento de probabilidad de complicaciones en DM1 (retinopatía, nefropatía, accidente cerebrovascular) si disminuye el TITR, estableciendo incluso porcentajes de riesgo (10). También empiezan a aparecer estudios que establecen una relación entre TITR y retinopatía diabética en adultos con DM2 e incluso otros autores describen que menores TITR se asocian con un riesgo aumentado de todas las causas de mortalidad cardiovascular en pacientes con DM2.
EN CONCLUSIÓN
- Tanto GRI como TITR son parámetros relativamente nuevos que pueden tener aplicabilidad clínica, aunque se necesitan estudios a mayor plazo que definan su utilidad, así como sus valores objetivo en distintos grupos poblacionales.
- Aunque el TIR continúa siendo el principal parámetro de seguimiento junto a la HbA1c para evaluar el riesgo potencial de complicaciones crónicas, el TITR puede ser una métrica adicional para evaluar el control glucémico, de especial importancia cuando la normoglucemia es un objetivo clínico.
- El GRI al tratarse de un parámetro único y fácil de calcular puede ser especialmente útil a aquellos profesionales con menor experiencia en la interpretación de MCG, y cuando se necesite para priorizar la atención a aquellos pacientes con peor control glucémico.
BIBLIOGRAFÍA
- Klonoff DC, Wang J, Rodbard D, Kohn MA, Li C, Liepmann D, et al. A Glycemia Risk Index (GRI) of Hypoglycemia and Hyperglycemia for Continuous Glucose Monitoring Validated by Clinician Ratings. J Diabetes Sci Technol. 2023 Sep;17(5):1226-1242. doi: 10.1177/19322968221085273. Epub 2022 Mar 29. PMID: 35348391; PMCID: PMC10563532.
- Díaz-Soto G, Pérez-López P, Férnandez-Velasco P, Nieto de la Marca MO, Delgado E, Del Amo S, et al. Glycemia Risk Index Assessment in a Pediatric and Adult Patient Cohort With Type 1 Diabetes Mellitus. J Diabetes Sci Technol. 2024 Sep;18(5):1063-1069. doi: 10.1177/19322968231154561. Epub 2023 Feb 16. PMID: 36794818; PMCID: PMC11418463.
- Wang Y, Lu J, Ni J, Wang M, Shen Y, Lu W et al. Association between glycaemia risk index (GRI) and diabetic retinopathy in type 2 diabetes: A cohort study. Diabetes Obes Metab. 2023 Sep;25(9):2457-2463. doi: 10.1111/dom.15068. Epub 2023 Jun 23. PMID: 37353345.
- Bahillo-Curieses P, Fernández Velasco P, Pérez-López P, Vidueira Martínez AM, Nieto de la Marca MO, Díaz-Soto G. Utility of time in tight range (TITR) in evaluating metabolic control in pediatric and adult patients with type 1 diabetes in treatment with advanced hybrid closed-loop systems. Endocrine. 2024 Nov;86(2):539-545. doi: 10.1007/s12020-024-03881-6. Epub 2024 May 30. PMID: 38814372; PMCID: PMC11489309.
- Castañeda J, Arrieta A, van den Heuvel T, Battelino T, Cohen O. Time in Tight Glucose Range in Type 1 Diabetes: Predictive Factors and Achievable Targets in Real-World Users of the MiniMed 780G System. Diabetes Care. 2024 May 1;47(5):790-797. doi: 10.2337/dc23-1581. PMID: 38113453; PMCID: PMC11043222.
- Dunn TC, Ajjan RA, Bergenstal RM, Xu Y. Is It Time to Move Beyond TIR to TITR? Real-World Data from Over 20,000 Users of Continuous Glucose Monitoring in Patients with Type 1 and Type 2 Diabetes. Diabetes Technol Ther. 2024 Mar;26(3):203-210. doi: 10.1089/dia.2023.0565. PMID: 38444315; PMCID: PMC10877396.
- Battelino T, Alexander CM, Amiel SA, Arreaza-Rubin G, Beck RW, Bergenstal RM, et al. Continuous glucose monitoring and metrics for clinical trials: an international consensus statement. Lancet Diabetes Endocrinol. 2023 Jan;11(1):42-57. doi: 10.1016/S2213-8587(22)00319-9. Epub 2022 Dec 6. Erratum in: Lancet Diabetes Endocrinol. 2024 Feb;12(2):e12. doi: 10.1016/S2213-8587(24)00001-9. PMID: 36493795.ino TIR > 70
- Ohno T, Tsujino D, Nishimura R. Is there a target value for time in tight range for individuals with type 1 diabetes on MDI? Data from masked CGM. Expert Rev Endocrinol Metab. 2024 Nov;19(6):507-512. doi: 10.1080/17446651.2024.2400487. Epub 2024 Sep 5. PMID: 39235079.
- Beck RW. Is It Time to Replace Time-in-Range with Time-in-Tight-Range? Maybe Not. Diabetes Technol Ther. 2024 Mar;26(3):147-150. doi: 10.1089/dia.2023.0602. PMID: 38156959.
- Zhang Z, Wang Y, Lu J, Zhou J. Time in tight range: A key metric for optimal glucose control in the era of advanced diabetes technologies and therapeutics. Diabetes Obes Metab. 2025 Feb;27(2):450-456. doi: 10.1111/dom.16033. Epub 2024 Nov 11. PMID: 39529452.







