La retinopatía diabética (RD) es una microangiopatía retiniana que se desarrolla principalmente como consecuencia de la hiperglucemia crónica asociada o no a hipertensión arterial. Desafortunadamente seguimos pudiendo afirmar que la retinopatía diabética es la primera causa de ceguera en menores de 65 años en países occidentales.
Los hábitos alimenticios, el cambio en el estilo de vida de la población, el sedentarismo y la obesidad son algunos de los motivos que están derivando en el aumento de la incidencia de retinopatía diabética y de sus complicaciones. Mientras que otras causas de ceguera tales como cataratas ha disminuido, en el caso de la RD el número de invidentes se duplicó entre el 1990 y 2015 (1).
Tras más de 20 años de evolución de la enfermedad, el 90% de los casos de diabetes tipo 1 y el 60% del tipo 2, tendrían alguna forma de retinopatía, y de ellos, el 5% requerirá de tratamiento para evitar una ceguera irreversible.
TRAS MÁS DE 20 AÑOS DE EVOLUCIÓN DE LA ENFERMEDAD, EL 90% DE LOS CASOS DE DIABETES TIPO 1 Y EL 60% DEL TIPO 2, TENDRÍAN ALGUNA FORMA DE RETINOPATÍA, Y DE ELLOS, EL 5% REQUERIRÁ DE TRATAMIENTO PARA EVITAR UNA CEGUERA IRREVERSIBLE
Dado este panorama el enfoque de la RD debería estar centrado en tres aspectos:
1. Diagnóstico temprano de la enfermedad
El diagnóstico y manejo en la RD se basa en la identificación de los pacientes en riesgo antes de la pérdida de agudeza visual, este es el motivo por el que todos los pacientes deberían ser explorados de forma periódica por un oftalmólogo (Nivel de evidencia 1).
El problema de dicha recomendación sería la sobrecarga asistencial, ya que el 70% de las personas con diabetes no presentan signos de retinopatía DM.
Debido a la dimensión del problema se han puesto en marcha en algunos países programas de cribado mediante el uso de cámaras no midriáticas y telemedicina (sensiblidad ˃80% y especificidad ˃90%) (2). De forma que la primera retinografía debería realizarse a los 3-5 años del diagnóstico en DM tipo 1 y en el momento del diagnóstico en DM tipo 2 (1).
A posteriori, el cribado se realizará cada 2-3 años en personas con diabetes con menos de 10 años de evolución, buen control y sin RD; mientras que si estos criterios no se cumplen la retinografía debería ser anual o para aquellos con RD no proliferativa leve.
Este programa de cribado se ha implantado en numerosos países con éxito siendo realizado por oftalmólogos, en nuestro país RETISALUD en Canarias o en comunidad catalana que es realizado por médicos de Atención Primaria. Sigue siendo discutido el añadir a la retinografía la realización de una tomografía de coherencia óptica (Optical Coherence Tomography, OCT) macular de cribado, dada la especificidad de la técnica que requeriría personal experto, pero que cada vez está más presente en el diagnóstico y tratamiento.
Los programas de cribado basados en inteligencia artificial van a ocupar un lugar muy determinante en la RD habiendo demostrado en la actualidad altos valores de sensibilidad y especificidad. Hay publicados numerosos estudios que usan esta tecnología para priorizar el seguimiento de las visitas, y aunque han demostrado un gran potencial, hay que ajustar los protocolos a las prácticas clínicas reales (3).
LOS PROGRAMAS DE CRIBADO BASADOS EN INTELIGENCIA ARTIFICIAL VAN A OCUPAR UN LUGAR MUY DETERMINANTE EN LA RD HABIENDO DEMOSTRADO EN LA ACTUALIDAD ALTOS VALORES DE SENSIBILIDAD Y ESPECIFICIDAD
2. Control y prevención de la RD
En todos los estadios de RD el control endocrinológico se ha mostrado como el pilar fundamental, siendo criterios altamente relevantes:
- Controlar los niveles de glucosa en sangre: se debe mantener la hemoglobina glicosilada A1c (HbA1c) por debajo del 7%. Las personas con DM1 que mantienen este nivel reducen la incidencia de RD en un 76% y la progresión en un 54% según el Diabetes Control and Complications Trial (DCCT) (4). El control intensivo de la glucemia se asocia con la reducción del riesgo de aparición de RD y reducción de la RD existente tanto en DM tipo 1 como tipo 2 respecto al tratamiento convencional. Además, en el DCCT el control intensivo se asoció a reducción de la progresión de RDNP severa y de RDP, la incidencia de edema macular y la necesidad de panfotocoagulación (PFC) y fotocoagulación focal (4). Paradójicamente un control muy rápido de las glucemias puede provocar empeoramiento y edema macular que se relaciona con el grado más avanzado de RD y peor control de la DM previo a la terapia intensiva.
- Mantener los niveles de tensión arterial por debajo de 130/80. En cuanto a la hipertensión arterial (HTA) también asocia aumento de aparición de edema macular y progresión, por lo que su control también muestra un grado de evidencia A. Su control estricto disminuye la progresión en un 34% y el deterioro de la visión en un 47% (5). Los medicamentos que bloquean el sistema renina angiotensina disminuyen la incidencia de RD en pacientes con diabetes tipo 1 e inducen una regresión en aquellos con diabetes tipo 2 (6).
- Tener las cifras de colesterol LDL ˂100 mg/dl y triglicéridos ˂ 150 mgr/dl. El uso de atorvastatina no ha podido demostrar que influyera en la progresión de la RD. Sin embargo el uso de fenofibrato para el control de los triglicéridos si demostró efecto sobre la progresión y descenso de los pacientes que precisaban tratamiento mediante fotocoagulación (1).
- Otros factores de riesgo cardiovascular.
-
- En cuanto al estado renal se debe controlar la microalbúmina en orina.
- No fumar.
- Evitar el sobrepeso.
- Hacer ejercicio y seguir una dieta saludable. En relación al ejercicio físico se asocia a menor severidad de la RD.
Control estrecho en pacientes adolescentes. En los pacientes adolescentes el riesgo de desarrollar complicaciones es elevado, por lo que los pediatras deben intensificar sus revisiones; se ha visto que la terapia intensiva con insulina es especialmente útil en este grupo (7).
Clasificación de la RD y seguimiento
A fin de establecer unos criterios uniformes el Global Diabetic Rethinopathy Project Group (8) publicó en 2003 una clasificación:
- RD no proliferativa leve: se trata de la etapa inicial de la enfermedad. Aparecen los microaneurismas que son dilataciones de la pared de los pequeños vasos sanguíneos de la retina.
Requiere control oftalmológico o retinografía anual.
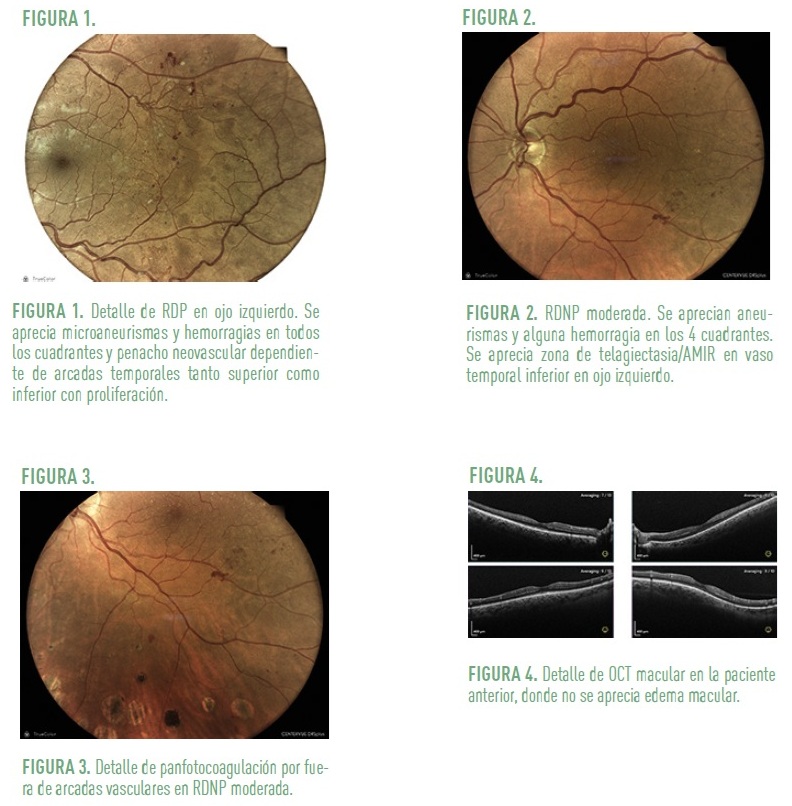
- RD no proliferativa moderada: presencia de microaneurismas asociados a menos de 20 hemorragias, exudados duros, y produciéndose también obstrucciones vasculares que aparecen como manchas blanquecinas denominadas exudados blandos.
Requiere control oftalmológico semestral.
- RD no proliferativa severa: presencia de microaneurismas añadido a uno de los siguientes:
-
- Más de 20 hemorragias en cada uno de los 4 cuadrantes.
- Arrosariamiento venoso en 2 o más cuadrantes.
- Anomalías microvasculares intraretinianas (AMIR) en 1 o más cuadrantes.
Requiere control oftalmológico en unidad especializada de retina, seguimiento cada 3 meses.
- RD proliferativa: presencia de crecimiento de nuevos vasos sanguíneos. Estos vasos sanguíneos crecen a lo largo retina y en la superficie del vítreo, y se rompen con facilidad provocando hemorragias prerretiniana o hemovitreo.
Seguimiento mensual.
La presencia de edema macular diabético (EMD) se puede clasificar en base a los hallazgos en OCT dado que se trata de un método objetivo y fiable, de forma sencilla según la guía del International Council of Ophthalmology:
- No edema macular (EM).
- EM de afectación no central: engrosamiento retiniano que no abarca la zona central (1mm de diámetro).
- EM de afectación central: engrosamiento de zona central.
3. Tratamientos
- La RD no proliferativa: requiere el control estricto de los factores de riesgo previamente mencionados.
En el caso de la forma severa o muy severa la PFC es el tratamiento de elección si el riesgo de progresión es notable.
- La RD proliferativa: en la actualidad el tratamiento con inyecciones intravitreas de anti-factor de crecimiento endotelial vascular (anti-vascular endothelial growth factor, anti-VEFG) de manera mantenida está aprobado en este estadio, sin embargo, la PFC sigue siendo el gold standard por los problemas de control y seguimiento de los pacientes que si sólo han recibido anti-VEFG puede tener consecuencias nefastas (hecho que no sucede con la PFC, al ser estable y duradero).
- Edema macular diabético.
Es la causa más frecuente de pérdida de visión de una persona con diabetes. Se trata de una complicación que puede aparecer tanto en pacientes con retinopatía diabética no proliferativa como en pacientes con retinopatía diabética proliferativa. Clínicamente se manifiesta como una pérdida de visión subaguda y con escotoma central.
El diagnóstico se basa en una funduscopia aunque cada vez con más frecuencia nos apoyamos de la OCT, ya que esta técnica además nos va a permitir cuantificar la cantidad de edema y monitorizar la respuesta al tratamiento de una manera objetiva.
El tratamiento fundamental del EMD se basa en inyecciones intravítreas. Existen dos grupos farmacológicos diferentes: antiVEGF y corticoides. Muchos pacientes precisan de la combinación de las dos líneas de tratamiento.
En cuanto a los antiVEGF, existen 4 fármacos aprobados para su uso en el EMD: ranibizumab, aflibercept, brolucizumab y faricimab. El bevacizumab se usa fuera de indicación por motivos económicos o cuando no se dispone o no han sido eficaces los que sí están aprobados.
Con respecto a los corticoides intravítreos, se puede usar el implante de dexametasona y el implante de acetónido de fluocinolona. Difieren entre ellos en su duración de acción y ambos pueden producir hipertensión ocular, glaucoma o desarrollo de cataratas.
En casos seleccionados, aunque actualmente en desuso, puede aplicarse tratamiento con láser focal Argón.
Conclusiones
- El aumento de la incidencia de la diabetes y de sus complicaciones metabólicas se ha convertido en un problema de salud que requiere abordaje estrecho y multidisciplinar.
- El despistaje de la RD con diagnóstico precoz es la única manera en la actualidad de controlar y prevenir las consecuencias de la RD.
- El control de los factores de riesgo cardivascular con especial interés en hemoglobina glicosilada y HTA ha demostrado mejorar el riesgo de progresión de la RD.
Bibliografía
- Guia 3. Manejo de las complicaciones oculares de la diabetes. Retinopatía diabética y edema macular. Guías de práctica clínica y monografías de la SERV. Copyright 2023. Sociedad española de Retina y Vitreo. .
- Wilson JM, Jungner YG. [Principles and practice of mass screening for disease]. Boletin de la Oficina Sanitaria Panamericana Pan American Sanitary Bureau. 1968 Oct;65(4):281-393. PubMed PMID: 4234760. Epub 1968/10/01. Principios y metodos del examen colectivo para identificar enfermedades. spa.
- Bora A, Tiwari R, Bavishi P, Virmani S, Huang R, Traynis I, et al. Risk Stratification for Diabetic Retinopathy Screening Order Using Deep Learning: A Multicenter Prospective Study. Translational vision science & technology. 2023 Dec 1;12(12):11. PubMed PMID: 38079169. Pubmed Central PMCID: PMC10715315 (I); P. Bavishi, Google (E), Alphabet (I); S. Virmani, Google (E), Alphabet (I); R. Huang, None; I. Traynis, None; G.S. Corrado, Google (E), Alphabet (I); L. Peng, Google (E), Alphabet (I); D.R. Webster, Google (E), Alphabet (I); A.V. Varadarajan, Google (E), Alphabet (I); W. Pattanapongpaiboon, None; R. Chopra, Google (E), Alphabet (I); P. Ruamviboonsuk, None. Epub 2023/12/11. eng.
- Nathan DM, Genuth S, Lachin J, Cleary P, Crofford O, Davis M, et al. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. The New England journal of medicine. 1993 Sep 30;329(14):977-86. PubMed PMID: 8366922. Epub 1993/09/30. eng.
- Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. UK Prospective Diabetes Study Group. BMJ (Clinical research ed). 1998 Sep 12;317(7160):703-13. PubMed PMID: 9732337. Pubmed Central PMCID: PMC28659. Epub 1998/09/11. eng.
- Sjølie AK, Klein R, Porta M, Orchard T, Fuller J, Parving HH, et al. Effect of candesartan on progression and regression of retinopathy in type 2 diabetes (DIRECT-Protect 2): a randomised placebo-controlled trial. Lancet. 2008 Oct 18;372(9647):1385-93. PubMed PMID: 18823658. Epub 2008/10/01. eng.
- Virk SA, Donaghue KC, Wong TY, Craig ME. Interventions for Diabetic Retinopathy in Type 1 Diabetes: Systematic Review and Meta-Analysis. American journal of ophthalmology. 2015 Nov;160(5):1055-64 e4. PubMed PMID: 26210869. Epub 2015/07/27. eng.
- Wilkinson CP, Ferris FL, 3rd, Klein RE, Lee PP, Agardh CD, Davis M, et al. Proposed international clinical diabetic retinopathy and diabetic macular edema disease severity scales. Ophthalmology. 2003 Sep;110(9):1677-82. PubMed PMID: 13129861. Epub 2003/09/18. eng.