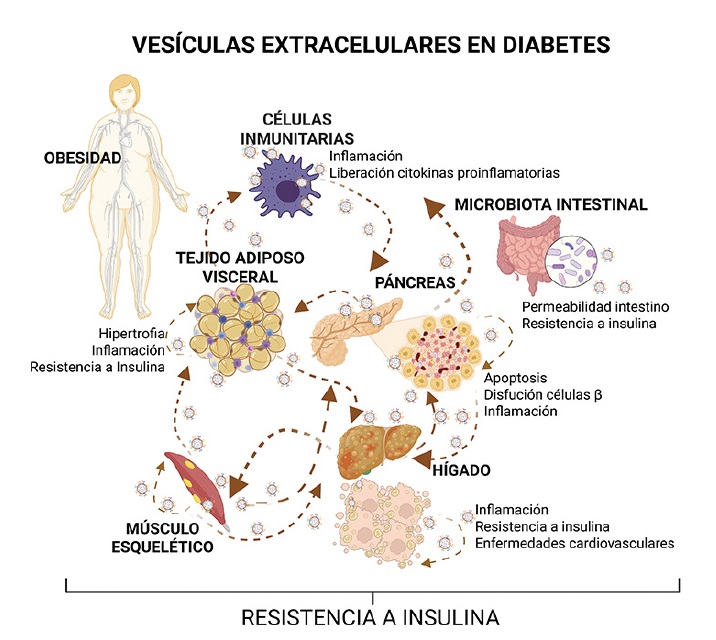
VESÍCULAS EXTRACELULARES EN DIABETES
Las vesículas extracelulares (VEs) son pequeñas nano esferas membranosas liberadas por todas las células del organismo y por lo tanto pueden encontrarse en cualquier fluido biológico como sangre, orina, lágrima y leche materna, entre otros. En función de su origen y tamaño, se pueden identificar hasta tres tipos distintos de vesículas, pudiéndose clasificar en microvesículas (100 nm – 1 µm) derivadas de la evaginación de la membrana plasmática celular, exosomas (30 – 100 nm) provenientes del interior de la célula y secretados por exocitosis, o vesículas más grandes (50 – 5000 nm) también denominadas cuerpos apoptóticos, liberadas por las células tras la muerte celular o apoptosis. En un principio se atribuía a estas vesículas la función de facilitar la eliminación de moléculas de deshecho celular, pero posteriormente, se redescubrieron como un nuevo mecanismo de comunicación intercelular alternativo a las vías clásicas de comunicación mediante moléculas solubles secretadas. Así, este nuevo mecanismo de comunicación se debe, en gran medida, a la composición de estas vesículas, que no solo llevan proteínas de membrana que pueden dirigirlas a una célula o tejido diana específica, sino que en su interior portan distintas moléculas bioactivas como proteínas, ADN y distintos ARNs. Este cargo molecular es precisamente lo que las hace tan interesantes, porque, por un lado, representan el estado fisiológico/patológico de la célula de origen, postulándose como valiosos reservorios de biomarcadores, y por otro, ejerciendo un papel funcional al interaccionar con las células o tejidos de destino. Esta interacción puede desencadenar una señal en el interior de la célula diana o incluso ejercer una modificación en la expresión de los genes mediante las moléculas de ARN que porta en su interior como los miARNs inhibidores. En concreto, en la diabetes, distintos miARNs que viajan en las VEs regulan vías de señalización vitales para preservar la sensibilidad a la insulina, por lo que desempeñan un papel en la aparición de resistencia a la insulina. Por lo tanto, las VEs se convierten en verdaderos caballos de Troya celulares capaces de influir sobre la función de células y tejidos no solo a nivel local, sino también a distancia al poder viajar por la sangre alcanzando incluso el cerebro.
LAS VESÍCULAS EXTRACELULARES LIBERADAS POR TODAS LAS CÉLULAS DEL ORGANISMO SE POSTULAN COMO VERDADEROS CABALLOS DE TROYA CELULARES PARTICIPANDO TANTO EN PROCESOS FISIOLÓGICOS NORMALES, COMO EN LA ENFERMEDAD
En las últimas décadas, las VEs han resurgido como actores clave en la comunicación entre células y tejidos abriendo nuevos campos en la investigación biomédica, dado que se han visto implicadas tanto en procesos fisiológicos normales, como en el transcurso de enfermedad (1). En concreto, en los últimos años, se han descrito múltiples funciones de estas vesículas en el establecimiento y desarrollo de enfermedades metabólicas, incluida la obesidad, y sus comorbilidades, donde destaca la diabetes tipo 2 (DM2) (2). La DM2 es una enfermedad metabólica crónica caracterizada por la elevación continuada de glucosa en la sangre debida a la resistencia a insulina en los tejidos periféricos y/o a la secreción insuficiente de insulina, debido a la muerte progresiva de células β en el páncreas, en la cual, también participa la inflamación crónica general de todo el organismo como consecuencia de la obesidad y el sedentarismo. Por todo ello, la diabetes tiene una repercusión muy importante para la salud pública ya que su incidencia y prevalencia están aumentando en todo el mundo.
VESÍCULAS EXTRACELULARES DEL TEJIDO ADIPOSO Y SU PAPEL EN DIABETES
La acumulación excesiva de grasa en el tejido adiposo durante el desarrollo de la obesidad se considera uno de los principales factores de riesgo de diabetes. Así, la alteración de este tejido está estrechamente relacionada con mecanismos asociados a esta enfermedad, como el desarrollo de resistencia a insulina (diabetes), inflamación y liberación de ácidos grasos. Pero ¿participan las VEs en estos procesos? Existen evidencias que muestran que, durante el desarrollo de la obesidad, las células encargadas de acumular energía (adipocitos) en el tejido adiposo liberan VEs al exterior que interaccionan con células vecinas sanas induciendo o empeorando por sí mismas la enfermedad (3, 4). Así, se ha descrito que estas vesículas secretadas por células del tejido adiposo obeso promueven la acumulación de lípidos (grasas) e inducen la resistencia a insulina (diabetes) en células del mismo tejido que aún están sanas (4). A su vez, se observó que las VEs liberadas por los adipocitos del tejido adiposo de personas que sufren obesidad son capaces de interaccionar con otras células presentes en el tejido adiposo. En concreto, se vio que las VEs de adipocitos de individuos con obesidad, son capaces de interaccionar con células del sistema inmune como macrófagos y linfocitos que van invadiendo la grasa en esta enfermedad (5). Esta interacción promueve su inflamación, y por tanto forzando la liberación de señales proinflamatorias responsables no solo de la inflamación local, sino que también podrían participar en la inflamación a nivel global del organismo. En concreto, se ha descrito que, en humanos, los adipocitos presentes en la grasa visceral (depositada a nivel abdominal entre los órganos), considerada más deletérea, liberan VEs con mayor capacidad inflamatoria que los liberados por la grasa subcutánea, localizada debajo de la piel (5, 6). Esta inflamación de bajo grado continuada, asociada a la obesidad, se sabe que interfiere en la señalización de la insulina, el metabolismo de la glucosa y la homeostasis lipídica, todo ello, contribuyendo a la resistencia a la insulina y la diabetes. Por ello, se postula, que las VEs podrían estar jugando un papel importante en el desarrollo de la resistencia a insulina promovida por inflamación. Las evidencias experimentales indican que las VEs establecen un diálogo dinámico entre adipocitos y macrófagos en el tejido adiposo participando en el proceso inflamatorio mencionado. A su vez, diversos trabajos muestran que los macrófagos también liberan VEs que podrían inducir la resistencia a insulina de los adipocitos cercanos.
LAS VESÍCULAS EXTRACELULARES SURGEN COMO NUEVOS FACTORES DE RELEVANCIA EN LA DIABETES PARTICIPANDO ACTIVAMENTE EN LA DISFUNCIÓN DE LAS CÉLULAS β Y EN LA RESISTENCIA A INSULINA
Es importante destacar que las VEs del tejido adiposo no solo actúan a nivel local, sino que pueden alcanzar el torrente sanguíneo e interaccionar con otros órganos y tejidos participando en la resistencia a insulina e inflamación de estos. Se ha observado, que las VEs liberadas por adipocitos patológicos murinos, o de grasa visceral y subcutánea humana de pacientes con obesidad, provocan la resistencia a insulina en hepatocitos del hígado, especialmente aquellas que proceden de la grasa acumulada a nivel central o visceral (5).
VESÍCULAS EXTRACELULARES DEL HÍGADO EN DIABETES
Las VEs liberadas por el hígado desempeñan un papel importante en el desarrollo y la progresión de la diabetes. Estas VEs, liberadas por distintas células del hígado, pueden alterar la señalización de la insulina y aumentar la resistencia a la misma (7). Así, las VEs del hígado, sobre todo en la enfermedad del hígado graso no alcohólico asociado a la obesidad, al igual que ocurre en el tejido graso, pueden promover la inflamación activando los macrófagos y liberando citoquinas proinflamatorias. Esta inflamación contribuye a la resistencia a la insulina y daña aún más el hígado. Se ha visto, además, que estas vesículas hepáticas pueden alterar la función de las células que recubren los vasos sanguíneos contribuyendo al desarrollo de complicaciones de la diabetes como las enfermedades cardiovasculares. Además, pueden viajar por el torrente sanguíneo alcanzando otros tejidos como el adiposo, el páncreas y el músculo pudiendo amplificar los efectos de la resistencia a la insulina y contribuir al desarrollo de la diabetes. Por el contrario, recientemente se ha descrito que VEs del hígado en condiciones normales no patológicas podrían tener potencial como terapia, ya que actúan en tejidos periféricos regulando los niveles de glucosa tras la ingesta (8).
VESÍCULAS EXTRACELULARES DEL PÁNCREAS Y DIABETES
El deterioro de la función o la cantidad de células β a medida que avanza la diabetes está relacionado con una compleja red de comunicación entre las células de los islotes pancreáticos y otras células y tejidos periféricos. Los factores estresantes asociados a la diabetes, incluidas las citocinas proinflamatorias, la toxicidad por lípidos y glucosa, y los depósitos de las proteínas amiloides, pueden alterar el microambiente de los islotes, influyendo en la carga molecular de las VEs secretadas por las células β en el páncreas provocando cambios funcionales (9). Por ello, las VEs derivadas de los islotes pancreáticos desempeñan un papel importante en la patogénesis de la diabetes al mediar en la comunicación entre órganos e influir en la función de las células β. Por ejemplo, estudios postulan que las células β pancreáticas prediabéticas liberan VEs con un ARN inhibidor (miR-29) capaz de inflamar células del sistema inmune, aumentando la resistencia a insulina. Posteriormente, en fases tardías de diabetes, se ha observado que la comunicación mediada por las VEs entre los islotes pancreáticos y otros tejidos puede conducir a la apoptosis y la disfunción de las células β. Por otro lado, se ha descrito que vesículas liberadas por células β pancreáticas tratadas con colesterol LDL pueden inducir un deterioro de la señal de insulina y provocar resistencia a la misma en el hígado. A su vez, las VEs derivadas del hígado graso pueden aumentar la infiltración de células inmunitarias en el páncreas y el consiguiente fallo de las células β.
En resumen, el páncreas es tanto el órgano afectado por el daño diabético como la fuente de VEs patógenas que facilitan la comunicación entre el páncreas, órganos distantes y el sistema inmunitario. Por todo ello, las VEs procedentes del islote pancreático o dirigidas a él pueden influir en la regulación fisiológica de la homeostasis de las células β, así como en las reacciones fisiológicas o patológicas al estrés.
VESÍCULAS EXTRACELULARES DE OTROS TEJIDOS Y ORGANISMOS
El músculo esquelético desempeña un papel crucial en el equilibrio de los niveles de glucosa; por ello, la resistencia a la insulina en este tejido es un factor clave en la diabetes. Se ha demostrado que el ejercicio regular reduce la incidencia de diabetes tipo 2, y que la interacción entre el músculo esquelético y las células β es esencial para este efecto; de hecho, las VEs liberadas por el músculo esquelético tras el ejercicio tienen efectos positivos en el páncreas (2). En el contexto de la resistencia a la insulina inducida por lípidos, las VEs que se originan en las células del músculo esquelético se cargan con los ácidos grasos saturados pudiendo alcanzar tejidos que responden a la insulina, como el páncreas y el hígado, lo que pone de manifiesto una nueva forma de comunicación entre órganos y de equilibrio metabólico.
En cuanto a otros organismos, es cada vez más patente que el desequilibrio del microbiota intestinal contribuye significativamente a la diabetes al causar metabolitos intestinales irregulares y alterar la permeabilidad del intestino (10). Estudios en ratones sugieren que las VEs liberadas por una bacteria beneficiosa del intestino (Akkermansia muciniphila), podrían prevenir la resistencia a la insulina ya que consiguen contrarrestar los efectos nocivos sobre la permeabilidad del intestino inducida por una dieta rica en grasa. En general, la alteración de la barrera intestinal asociada a la obesidad y diabetes conduce a un aumento de las VEs procedentes de las bacterias intestinales que circulan por todo el organismo exacerbando la resistencia a la insulina.
CONCLUSIÓN
Las vesículas extracelulares liberadas por todas las células del organismo se postulan como verdaderos caballos de Troya celulares participando tanto en procesos fisiológicos normales, como en la enfermedad. En concreto, las VEs surgen como nuevos factores de relevancia en la diabetes participando activamente tanto en la disfunción de las células β como en la resistencia a insulina. A su vez, en condiciones patológicas como la obesidad, distintos órganos periféricos como el tejido adiposo, músculo e hígado, entre otros, liberan VEs propias, capaces de interaccionar con el páncreas alterando la función de la célula pancreática. Al contrario, las VEs de células no patológicas ejercen efectos beneficiosos, y surgen como herramientas terapéuticas prometedoras.
REFERENCIAS
- Qisong L, Jianghong H, Jiang X, Yujie L, Guangheng L. Tracking tools of extracellular vesicles for biomedical research. Front Bioeng Biotechnol. 2022;18 (10):943712.
- Zhang M, Wang L, Chen Z. Research progress of extracellular vesicles in type 2 diabetes and its complications. Diabetes Med. 2022; 39: e14865.
- Zhang B, Yang Y, Xiang L, Zhao Z, Ye R. Adipose-derived exosomes: A novel adipokine in obesity-associated diabetes. J Cell Physiol. 2019; 234:16692–702.
- Camino T, Lago-Baameiro N, Bravo SB, Sueiro A, Couto I, Santos F, et al. Vesicles shed by pathological murine adipocytes spread pathology: characterization and functional role of insulin resistant/hypertrophied adiposomes. Int J Mol Sci. 2020; 21:2252.
- Lago-Baameiro N, Camino T, Vazquez-Durán A, Sueiro A, Couto I, Santos F, et al. Intra and inter-organ communication through extracellular vesicles in obesity: functional role of obesesomes and steatosomes. J Transl Med. 2025;23(1):207.
- Camino T, Lago-Baameiro N, Bravo SB, Molares-Vila A, Sueiro A, Couto I et al. Human obese white adipose tissue sheds depot-specific extracellular vesicles and reveals candidate biomarkers for monitoring obesity and its comorbidities. Transl Res. 2022; 239:85-102.
- Liu Z, Yin R, Tian J. Extracellular vesicles: mechanisms and prospects in type 2 diabetes and its complications. Front Endocrinol. 2025 17; 15:1521281.
- Miotto PM, Yang C-H, Keenan SN, De Nardo W, Beddows CA, Fidelito G et al. Liver-derived extracellular vesicles improve whole-body glycemic control via inter-organ communication. Nature Metabolism. 2024; 6(2):1-19.
- Wei J, Wang Z, Han T, Chen J, Ou Y, Wei L et al. Extracellular vesicle-mediated intercellular and interorgan crosstalk of pancreatic islet in health and diabetes. Front Endocrinol. 2023; 25:14:1170237.
- Barathan M, Luan Ng S, Lokanathan Y, Hwei Ng, Law JX. The profound influence of gut microbiome and extracellular vesicles on animal health and disease. Int J Mol Sci 2024;25(7):4024.